Lifestyle
Alimentos procesados: la explicación científica de por qué nos enganchamos a ellos

Comida rápida. Foto. El Mundo.
Comer mal está ligado a los altos índices de obesidad y desencadena otras patologías. Más allá del entrenamiento de los hábitos saludables, hay complejos procesos en el cerebro que nos llevan a una mala alimentación.
Cuanto peor comemos, más ganas de seguir. Si uno come una hamburguesa, lo asocia a patatas y refresco. Si sale de picoteo junto a unas bravas o unas tapas ‘el cuerpo le pide’ una cerveza. Y así todo. Un círculo vicioso del que nuestro cerebro se convierte en una presa. Y de nada vale enumerar una y otra vez las virtudes de una alimentación saludable, si el origen está en los complejos mecanismos de la neurobiología.
Por eso, los científicos buscan las claves en las neuronas. ¿Qué mecanismos son los que promueven unos hábitos u otros? Una investigación publicada en PNAS es de las últimas que intenta ofrecer una respuesta. La autora de la misma, Michiru Hirasawa, de la Universidad Memorial de Terranova (Canadá), está especializada en conocer los mecanismos fundamentales que subyacen a la regulación del peso corporal por parte del cerebro.
La abundancia de dietas sabrosas y ricas en grasas en las sociedades modernas ha contribuido al aumento epidémico de la obesidad, como recoge la publicación. Se cree que esto se debe en parte a la inflamación inducida por HFD en el hipotálamo, una región del cerebro crítica en el equilibrio energético.
Sin embargo, no queda claro cómo la inflamación, típicamente asociada con la enfermedad, puede causar un aumento de peso excesivo. Aquí, “mostramos que una molécula inflamatoria prostaglandina E2 es inducida en el hipotálamo por las dietas ricas en grasas y activa directamente un grupo de neuronas promotoras del apetito”, resume Hirasawa en el trabajo. El trabajo ha analizado este esquema en un modelo animal.
“El bloqueo de esta activación protege a los ratones de la obesidad y el hígado graso. Esto identifica un vínculo directo entre la inflamación hipotalámica y el aumento de peso, lo que puede servir como un posible objetivo terapéutico para la obesidad y el síndrome metabólico”, apunta la investigadora.
Desde el punto de vista de la neurobiología se intenta dar respuesta al patrón adaptativo obesogénico (PAO) donde el funcionamiento del sistema nervioso se organizaría tempranamente aumentando la ingesta como principal regulador del estrés. En un trabajo de la Universidad de Chile propone el patrón como un modelo de comprensión basado en la ausencia de integración precoz entre los diversos sistemas que regulan el eje HPA (hipotálamo-pituitaria-adrenal).
“Sería una respuesta maladaptativa establecida tempranamente que liga preferentemente los sistemas de recompensa a la modulación del eje HPA en ausencia de suficiente regulación social y que podría explicar la obesidad temprana infantil”. Es decir, asociar desde la infancia una dieta rica en grasas, normalmente variada en ultraprocesados, con una respuesta positiva frente a situación de estrés.
¿Cuál es el impacto de la obesidad en el mundo?
Los datos de la obesidad a nivel mundial son alarmantes. El Atlas Mundial de Obesidad 2023, publicado por la Federación Mundial de Obesidad, ya predice que el impacto económico global alcanzará los 4,32 mil millones de dólares al año en 2035 si no se ponen medidas. Esto supone casi el 3% del PIB mundial, cifras similares al impacto de Covid-19 en 2020.
La mayoría de la población mundial (51%, o más de cuatro mil millones de personas) vivirá con sobrepeso u obesidad para 2035 si prevalecen las tendencias actuales: una de cada cuatro (casi dos mil millones) desarrollará obesidad. Y las enfermedades que van de su mano: diabetes tipo 2, hipertensión, accidente cerebrovascular, cáncer, depresión, etc.
Para 2035 podría duplicarse el impacto en la población infantil respecto a 2020. Se prevé que las tasas crezcan más entre las niñas que entre los niños. Además, el Atlas Mundial de Obesidad 2023 muestra que el incremento es más acelerado entre la población infantil respecto a la adulta. Lo que significa que vivirán más años con enfermedades asociadas y se elevará el riesgo patológico.
El objetivo que persigue el equipo de Hirasawa es combatir la obesidad a través de la determinación de los mecanismos celulares-moleculares que subyacen al control central del balance energético (ingesta de alimentos y gasto energético), lo que se traducirá en nuevas dianas terapéuticas para la obesidad y los trastornos alimentarios.
¿Qué se busca en el cerebro para frenar la obesidad?
No es el primer estudio que busca respuestas en el cerebro. La ingesta de alimentos está regulada por mecanismos complejos que involucra a los circuitos del hipotálamo y el rombencéfalo. Esto ya se ha apuntado en varios trabajos.
Dada la relación de la obesidad con otras patologías, una investigación publicada en Molecular Psychiatry del Centro de Investigación de Ingeniería de Imágenes Moleculares y Neurológicas de la Universidad Xidian y el Laboratorio de Neuroimagen del Instituto Nacional sobre Abuso de Alcohol y Alcoholismo de Bethesda realizó una revisión sobre los cambios neuronales que se dan en personas obesas. La evidencia acumulada de los estudios de neuroimagen sugiere que “la obesidad afecta negativamente la función y la estructura del cerebro, especialmente dentro del circuito fronto-mesolímbico”, concluyen los autores.
En este trabajo se apunta que “las personas obesas muestran respuestas neuronales anormales a las señales de los alimentos, el gusto y el olfato, la actividad en estado de reposo y la conectividad funcional, y las tareas cognitivas que incluyen la toma de decisiones, el control inhibitorio, el aprendizaje/memoria y la atención. Además, la obesidad se asocia con una morfometría cortical alterada, un volumen reducido de materia gris-blanca y una integridad deficiente de la materia blanca”.
¿Qué se conoce de cómo se regulan los patrones alimentarios?
Las evidencias que muestran que los sistemas de recompensa también son importantes en la regulación del comportamiento alimentario. En este contexto, la amígdala se considera un área extra-hipotalámica clave que regula el comportamiento alimentario en humanos y roedores. Una revisión en Behavioural Brain Research se centra en la regulación de la ingesta de alimentos por parte de la amígdala y los mecanismos de resistencia a la insulina en esta área del cerebro.
Las autoras de la Universidad de Medicina de Campinas exponen estos complicados mecanismos (también en modelos murinos) que la dieta rica en grasas y los ácidos grasos saturados inducen, como la inflamación, estrés del ER (retículo endoplásmico) y la activación de serina quinasas como PKC (proteína quinasa C theta), JNK (c-Jun N-terminal quinasa) e IKK (inhibidor del factor nuclear kappa). Los datos sugieren que el estrés de PKC y ER son los principales mecanismos de resistencia a la insulina en la amígdala de ratas obesas y juegan un papel importante en la regulación del comportamiento alimentario.
-

 Nacionales
Nacionales1° de marzo: Mariscal López, la reivindicación de un héroe
-

 Deportes
DeportesCopa Intercontinental: 45 años de la mayor conquista de Olimpia
-

 Nacionales
NacionalesCiudad “joven y feliz”: Fernando de la Mora celebra este viernes 86 años de fundación
-

 Destacado
DestacadoComepar denuncia a directora que evidenció irregularidades en almuerzo escolar
-

 Destacado
DestacadoFuga de amoníaco en frigorífico Minerva Foods en San Antonio
-
 Nacionales
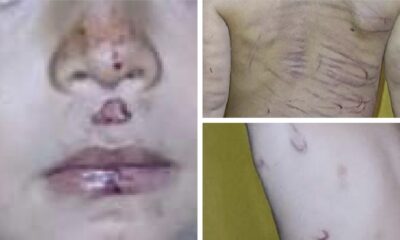
NacionalesNiño de 3 años fue brutalmente golpeado por su padrastro con un cinto y un cable
-

 Destacado
DestacadoMinerva Foods: Municipalidad dispone clausura y cancelación de patente tras fuga de amoníaco
-

 Nacionales
NacionalesTras terrrible ola de calor, anuncian ingreso de frente frío desde la próxima semana

















